- La revista
- adidas velcro sneaker for kids shoes boys size 1
- Платье, adidas Core 18 Длинные брюки , платье adidas — цена 598 грн в каталоге Короткие платья ✓ Купить женские вещи по доступной цене на Шафе, Украина #121602964
- Sneakers Draked Viola
- 👟 кроссовки adidas streetball cordura адидас / наложка bs👟 — цена 2540 грн в каталоге Кроссовки ✓ Купить мужские вещи по доступной цене на Шафе , adidas Originals Sustainable Stan Smiths Vita sneakers med heltäckande grafiskt mönster , Украина #126359384
- Nike LeBron Zoom Soldier VII (7) 'Deep Royal Blue' , Nike va t-il rééditer toutes les Air Force 1 B , IetpShops
- Nike Kyrie 8 DC9134 001 Release Date 4
- cheap nike sb dunk high new york mets cloud grey rush blue team orange white 2022 for sale dh7155 001
- air jordan 1 mid crater grey
- a ma maniere air jordan 1 high do7097 100 release date
- buy nike dunk low purple pulse dm9467 500 shoes online
- Presentación
- Políticas y proceso editorial
- Rigor científico y metodológico
- Producción y Administración
- Comités
- Normas presentación
- Consideraciones eticas
- Enviar artículo
- Hemeroteca
- Indexación
- Buscar
- Contacto
Farm Comunitarios. 2018 Dec 28;10(4):29-32. doi: 10.5672/FC.2173-9218.(2018/Vol10).004.06
¿Conocemos todas las interacciones farmacológicas?: el transportador OATP1B1
Introducción
La incidencia de las enfermedades crónicas guarda una relación directamente proporcional al creciente envejecimiento de la población. Es muy frecuente observar en la población anciana la coexistencia de comorbilidades que derivan a la prescripción de varios medicamentos. También, otros factores demográficos y socio sanitarios (sexo, nivel cultural, situación económica, prescripción inapropiada o intervención de varios médicos, etc.) contribuyen a que el paciente anciano sea más susceptible a la polifarmacia con el consiguiente riesgo de presentar interacciones farmacológicas, además de las reacciones adversas propias de cada medicamento (1,2).
La polimedicación constituye en definitiva un problema de salud pública. Esta situación desencadena una serie de consecuencias negativas, tales como el mayor riesgo de caídas y hospitalización, de hecho, estudios recientes han estimado entre un 10-20% de los ingresos hospitalarios es debido a una interacción medicamentosa (3).
Las interacciones se definen como alteraciones de la actividad o efecto de un fármaco, tanto a nivel cualitativo como cuantitativo, y pueden surgir como consecuencia de una interacción fármaco-alimento, fármaco-fármaco y/o fármaco-complemento dietético o planta medicinal.
Como se observa en la figura 1, las interacciones las podemos clasificar atendiendo a su naturaleza en:
1. Interacciones fisicoquímicas: aquellas que atañen a los aspectos galénicos durante la fabricación del medicamento (la solubilización de la forma farmacéutica…) y que, posteriormente, afecta a la liberación del principio activo.
2. Interacciones farmacológicas que, a su vez se subdividen en:
2.1. Interacciones farmacodinámicas, aquellas que tienen lugar en la biofase. Un fármaco interfiere en la actividad del otro al actuar en el mismo lugar de acción (receptor, enzima, etc.), siendo las posibles respuestas (tabla 1):
2.1.1. Sinergismo de suma: aumenta la actividad farmacológica debido a la suma de los efectos individuales de cada fármaco.
2.1.2. Sinergismo de potenciación: igualmente aumenta la actividad farmacológica, en este caso el efecto es superior a la suma de los efectos de cada fármaco implicado.
2.1.3. Antagonismo: se produce una reducción o anulación del efecto del fármaco, debido a la interacción.
2.2. Interacciones farmacocinéticas. Estas interacciones se producen porque un fármaco modifica los procesos a nivel de la absorción, distribución, metabolismo o excreción de otro fármaco.
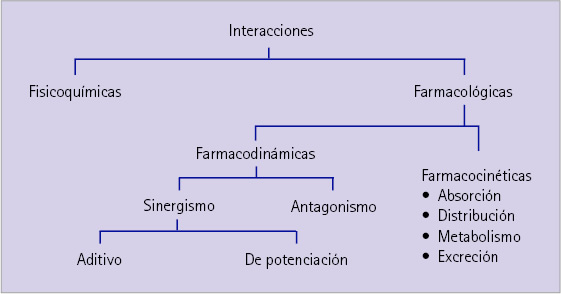
Figura 1 Clasificación de las interacciones con medicamentos
Tabla 1 Tipos de interacciones farmacodinámicas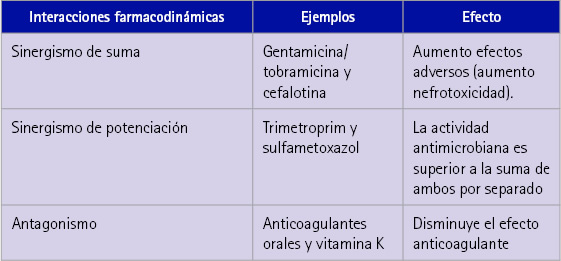
En la tabla 2 se ilustra la etapa farmacocinética implicada del proceso ADME así como las modificaciones que pueden llevar a cabo algunos fármacos en cada una de las etapas:
En cuanto a las interacciones con alimentos, un ejemplo clásico es la administración conjunta de IMAO (inhibidores de la mono-aminoxidasa mitocondrial) con alimentos ricos en tiramina, como el queso, que desencadena una crisis hipertensiva, una reacción adversa de relevancia clínica.
También puede disminuir el efecto del fármaco, como es el caso de la administración de la tetraciclina con un vaso de leche como consecuencia de la formación de un complejo insoluble con el calcio que impide la absorción del antibiótico.
También, debido al tratamiento concomitante de un fármaco con un complemento dietético, como es el caso de la Hierba de San Juan con inhibidores selectivos de la recaptación de la serotonina, puede desencadenar síndrome serotoninérgico (4).
Tabla 2 Tipos de interacciones farmacocinéticas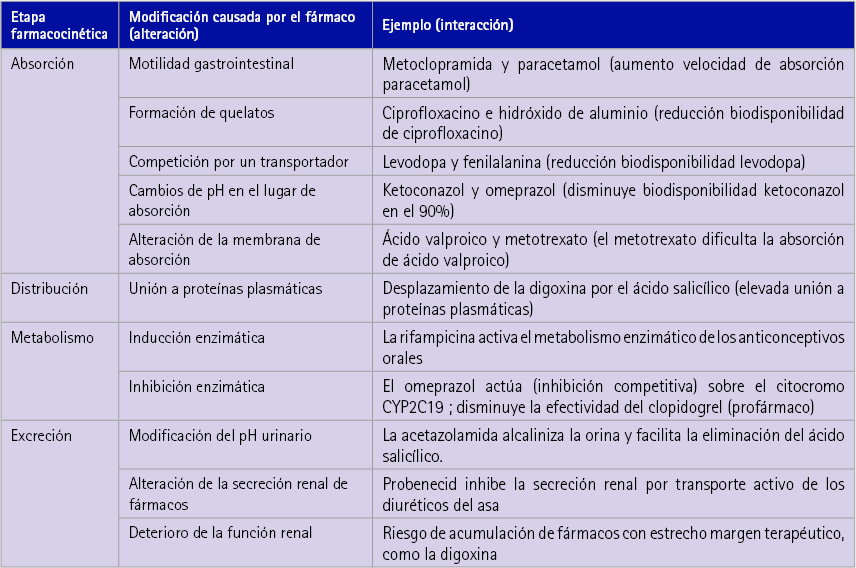
Objetivos
Realizar una revisión general sobre las interacciones farmacológicas centrándonos, en primer lugar, en abordar los diferentes tipos de interacciones implicadas en el fracaso terapéutico.
Revisar el papel del transportador OATP1B1 (transportador de aniones orgánicos polipeptídicos) en el metabolismo de fármacos.
Explicar el mecanismo de interacción entre la Rosuvastatina y el Olmesartán que deriva en una miositis.
Metodología
En el presente trabajo se ha llevado a cabo una revisión bibliográfica en la base de datos PubMed en la que se introdujeron las palabras clave “OATP1B1 and interactions” con el objetivo de encontrar artículos centrados en el papel del transportador OATP1B1 en el metabolismo de los xenobióticos y buscar una explicación a la interacción entre la Rosuvastatina (estatina) y el Olmesartán (ARA-II).
Se excluyeron todos aquellos artículos que no estaban relacionados con el transportador objeto de estudio (OATP1B1) y que se centraban exclusivamente en la farmacogenética y en los polimorfismos del OATP1B1 puesto que para este artículo nos interesa el papel que desempeña en el metabolismo de fármacos, las interacciones más relevantes y sus consecuencias a nivel clínico.
También se recopiló información en revistas especializadas en el área de la salud para obtener información sobre la situación actual de los pacientes ancianos polimedicados, en: BOTPlus web, Revistas Elsevier y Geriatricarea. Además, se recurrió a la base de datos Dialnet para encontrar información generalizada sobre las interacciones farmacológicas.
Resultados y discusión
Desde que aparece el primer artículo publicado sobre OATP1B1 en el año 2003 hasta nuestros días se han publicado 747 artículos sobre este transportador.
Las proteínas transportadoras de membrana de la familia OATP (Organic Anion Transporting Polypeptide) se han descubierto hace poco más de una década. Constituyen una subfamilia de los transportadores de membrana SLCO (Solute Carrier Organic Anion)
Están implicadas en interacciones farmacológicas de relevancia clínica y es una de las principales razones por las que varias agencias reguladoras, entre ellas la FDA, recomiendan la evaluación de nuevos fármacos en cuanto al grado de interacción a través de estos transportadores.
Dada la importancia de los OATPs se han revisado estudios recientes para entender mejor el mecanismo de interacción entre la Rosuvastatina y el Olmesartán y, también, para comprender cómo funcionan estos transportadores.
Aparecen publicados en Pubmed 83 artículos con las palabras clave OATP1B1 y rosuvastatine y 6 artículos con las palabras clave OATP1B1 y olmesartan y 0 artículos para la combinación con las palabras clave OATP1B1, olmersartan y rosuvastatine.
Las OATP desempeñan un papel importante en la extracción hepática de xenobióticos para su posterior biotransformación y eliminación. Por tanto, se caracterizan por ser unos transportadores secretores y afluentes, que facilitan la captación de sustancias endógenas (sales biliares, hormonas tiroideas…) y de numerosos medicamentos. Las distintas configuraciones que adoptan las proteínas de las OATP originan una serie de isoformas que se clasifican atendiendo a su localización tisular y fármacos que utilizan como sustrato, como se ilustra en la tabla 3 (5).
Tabla 3 Proteínas que participan en el transporte de ciertos fármacos, y por tanto modifican la absorción, distribución, metabolismo y eliminación de estos
Tabla 3 Proteínas que participan en el transporte de ciertos fármacos, y por tanto modifican la absorción, distribución, metabolismo y eliminación de estos 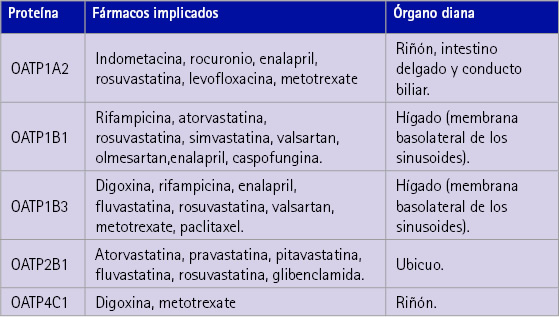
Actualmente, aún no se ha dilucidado el mecanismo de transporte de los OATPs. Sin embargo, diferentes estudios que se han llevado a cabo en estos últimos años apuntan a que el transporte de sustratos mediado por OATP se rige por un transporte activo secundario en el que interviene el bicarbonato como contraión para favorecer la entrada del sustrato al hepatocito (6,7).
Puesto que se trata de un transporte activo sigue una cinética de Michaelis-Menten. La velocidad de eliminación hepática resulta limitada, y como consecuencia su inhibición por un sustrato competidor, como un fármaco, es un factor crucial y determinante en la aparición de interacciones farmacológicas. De hecho, los estudios que se han revisado apuntan a que actualmente la postura más aceptada es la de una inhibición competitiva del transportador OATP1B1 que afecta a las propiedades farmacocinéticas de un determinado fármaco (7). El estudio dirigido por Alam K en el presente año señala que varios artículos se han enfocado recientemente en la importancia del transportador OATP1B1 en las interacciones farmacológicas con estatinas. Se ha visto que la administración conjunta de las estatinas con fármacos inhibidores del OATP1B1 incrementa los niveles plasmáticos de las estatinas, tal como reflejan los parámetros farmacocinéticos del área bajo la curva (AUC) y la concentración plasmática máxima (Cmax), que se encuentran aumentados cuando se inhibe el transportador. Esto puede generar efectos adversos clínicamente significativos como la miopatía, y la rabdomiolisis, que resulta mortal en casos graves.
Entre los fármacos que inhiben a OATP1B1 se encuentra el Olmesartán, como se observa en la tabla 3 y así lo refiere, también, el artículo de revisión de Alam K.
Estos hechos apoyan la posibilidad de que la tendinitis del paciente debido a una rotura del tendón de Aquiles, y que persistía a pesar de haber realizado varias sesiones de fisioterapia, resultara de una interacción entre el Olmesartán, que actúa como inhibidor del OATP1B1 con la Rosuvastatina (en la tabla 3 se observa también que utiliza el transportador OATP1B1).
Conclusión
Tras evaluar todos los datos obtenidos y analizar todos los factores que interactúan con el transportador OATP1B1 se concluye que puede producirse una interacción entre el Olmesartán y la Rosuvastatina. Esta interacción se debe a que el Olmesartán parece ser un inhibidor competitivo del transportador OATP1B1, además de usarlo para su metabolismo, lo que afecta al metabolismo de la Rosuvastatina. Esto provoca un aumento de la concentración de la Rosuvastatina en sangre, con lo cual, debería reducirse la dosis de administración de Rosuvastatina. De esta manera, evitaríamos posibles efectos adversos derivados de la interacción.
Referencias bibliográficas
1. Anónimo. La importancia real de las interacciones. Panorama Actual Med 2001; 25(245): 583-590 [acceso noviembre 2018]. Disponible en: http://publicaciones.portalfarma.com/pam/245/revision_1.pdf
2. Garrido-Garrido EM, García-Garrido I, García-López-Durán JC, García-Jiménez F, Ortega-López I, Bueno-Cavanillas A. Estudio de pacientes polimedicados mayores de 65 años en un centro de asistencia primaria urbano. Rev Calid Asist. 2011; 26(2): 90-96.[acceso noviembre 2018]. Disponible en http://www.elsevier.es/es-revista-revista-calidad-asistencial-256-articulo-estudio-pacientes-polimedicados-mayores-65-S1134282X10001454
3. Teresa Molina López, María de la O Caraballo Camacho, Soledad López Rubio Juan CarlosDomínguez Camacho, Juan Carlos Morales Serna. Prevalencia de polimedicación y riesgo vascular en la población mayor de 65 años. Atención Primaria 2012; 44 (4):216-222 [acceso noviembre 2018]. Disponible en https://www.sciencedirect.com/science/article/pii/S021265671100360X
4. Barcia-Hernández E, Negro-Alvarez S. Fundamentos de las interacciones farmacocinéticas. Anal Real Acad Farm. 2002; 68: 126-172. [acceso noviembre 2018]. Disponible en https://www.analesranf.com/index.php/aranf/article/viewFile/158/191
5. Ojeda GD. Papel de los transportadores en la Farmacología. 2015. [acceso noviembre 2018]. Disponible en: https://www.researchgate.net/publication/279181463_Papel_de_los_transportadores_en_la_Farmacologia
6. Russel FGM. Transporters: importance in drug absorption, distribution, and removal. En: K.S. Pang et al. (eds.), Enzyme and TransporterBased Drug–Drug Interactions. American Association of Pharmaceutical Scientists. 2010. DOI 10.1007/978-1-4419-0840-7_2 [acceso noviembre 2018]. Disponible en:
https://www.google.com/urlsa=t&rct=j&q=&esrc=s&souce=web&cd=1&ved=2ahUKEwNopTny4TfAhWjAhAIHS4ln8QFjAAegQIAxAC&url=htps%3A%2F%2Fwww.springercom%2Fcda%2Fcontent%2Fdcument%2Fcda_downloaddcument%2F9781441908391-c1pdf%3FSGWID%3D0-0-45-837961-p173906708&usg=AOvVaw0DnFOuPqNAUVWexMw_65wl
7. Alam K, Crowe A, Wang X, Zhang P, Ding K, Li L. Regulation of organic anion transporting polypeptides (OATP)1B1 and OATP1B3– mediated transport: an updated review in the context of OATP-mediated drug-drug interactions. 2018; Int J Mol Sci.. 19 (3), 855 [acceso noviembre 2018] Disponible en https://www.mdpi.com/1422 -0067/19/3/855
Editado por: © SEFAC. Sociedad Española de Farmacia Clínica, Familiar y Comunitaria.
© Copyright SEFAC. Sociedad Española de Farmacia Clínica, Familiar y Comunitaria. Este artículo está disponible en la url https://www.farmaceuticoscomunitarios.org/ Este trabajo está bajo la licencia Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License. Las imágenes u otro material de terceros en este artículo se incluyen en la licencia Creative Commons del artículo, a menos que se indique lo contrario en la línea de crédito. Si el material no está incluido en la licencia Creative Commons, los usuarios deberán obtener el permiso del titular de la licencia para reproducir el material. Para ver una copia de esta licencia, visite https://creativecommons.org/licenses/by-nc-nd/4.0/deed.es_ES


